239 利用VD1142修饰的精胺乙酰化葡聚糖对富含锌的氧化铜纳米粒子进行微流控封装以实现有效的癌症治疗按语
这篇由阿卡德米大学等的研究学者完成,讨论利用VD1142修饰的精胺乙酰化葡聚糖对富含锌的氧化铜纳米粒子进行微流控封装以实现有效的癌症治疗的论文,发表在一区重要期刊《Advanced Healthcare Meterials》,影响因子:5.609。
近年来,微波化学仪器用于材料合成的研究工作已经成为科学研究的热门方向,受到广大学者的极大关注!
摘要
纳米粒子的结构特征最近已经在不同类型的应用中被探索出来。探索纳米药物和物理摧毁癌症的具体粒子是很有趣的,这可能会避免癌症治疗中的许多障碍,例如耐药。
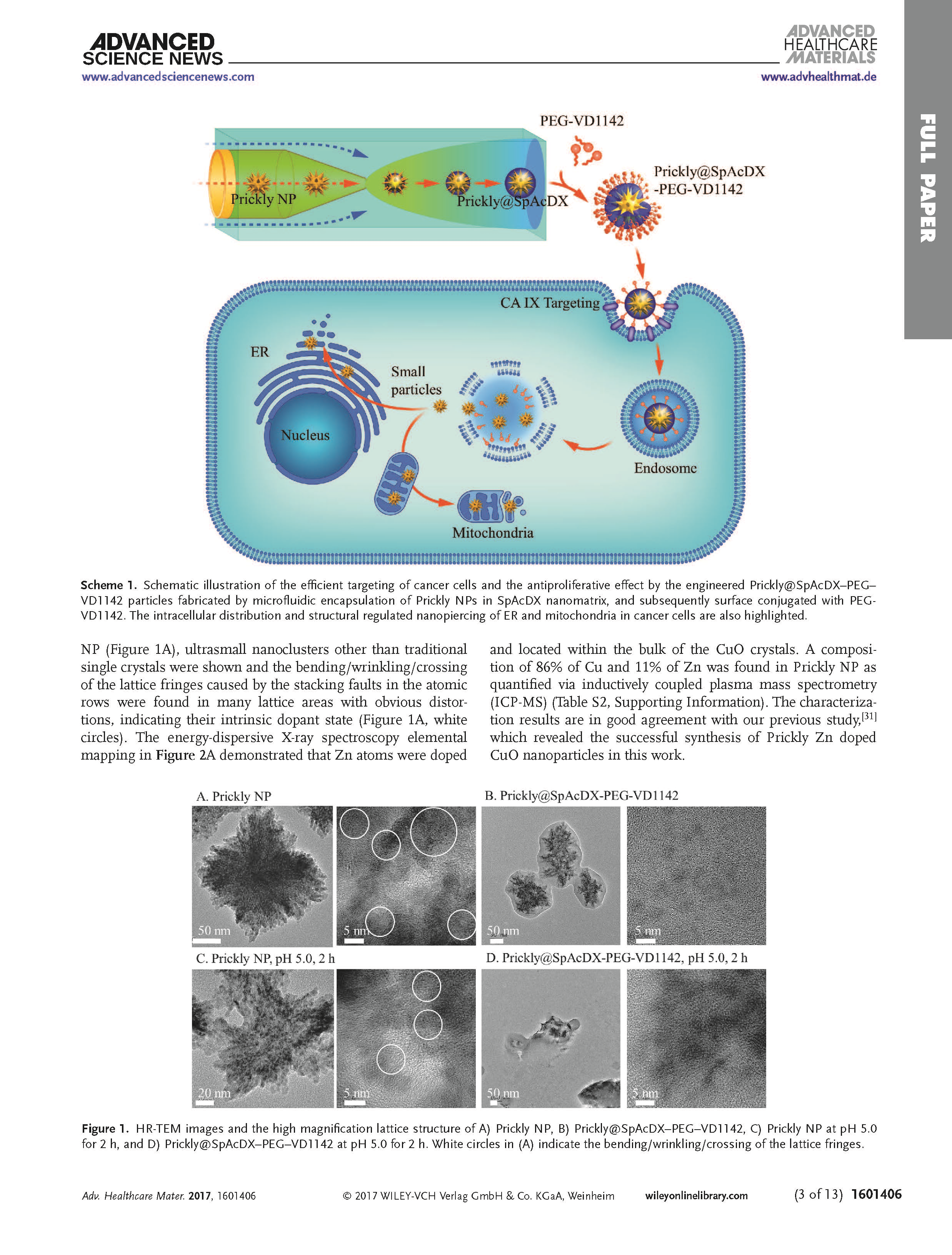
然而,这些系统的一个关键要素和技术挑战是有选择地针对癌细胞。作为概念的证明,合成了多刺锌掺杂氧化铜(Zn-CuO)纳米粒子,并将其封装在pH响应聚合物中;并用一种新的合成配体3-(环辛基氨基)-2,5,6-三甲基-4-[(2-羟乙基)磺酰基]苯磺酰胺(VD 1142)对其表面进行了改性,多刺NPs具有很强的抗肿瘤细胞增殖能力。
此外,聚合物包封屏蔽了多刺的纳米粒子,最重要的是,VP 1142将基因工程的NPs赋予碳酸氢酶IX,后者是一种跨膜蛋白,在多种肿瘤中都有过高表达。在细胞内,多刺的NPs分解成小块,在内质体逃逸时对细胞的内质网和线粒体造成严重的损伤。基因工程多刺NP在有效靶向治疗癌症方面具有广阔的应用前景,为纳米化开辟了新的途径。
详情


结论
总之,通过一种简单、环保的制备工艺,我们合成了多刺锌铜纳米粒子.多刺性NPs对DOX耐药乳腺癌细胞具有非常有效的抗癌作用。微fl纳米粒子沉淀成功地包封了多刺NPs,使其免受受体阴性细胞的非特异性损伤。此外,我们还研究了一种新型配体VP 1142对CAIX过表达的低氧MCF-7乳腺癌细胞的靶向性,并成功地证实了Pickly@SpAcDX-PEG-VD 1142对CAIX过表达的低氧MCF-7乳腺癌细胞的靶向选择性。具体来说,NPs在细胞内的分布表明,Pickly@SpAcDX-PEG-VD 1142诱导了细胞内小体的逃逸,更重要的是,它们分解成小块,通过纳米粒子的作用破坏了细胞内的ER和线粒体结构。通过对细胞凋亡蛋白标记物的评价和结构相关细胞死亡的比较,进一步认为肿瘤的抗肿瘤机制主要是由于细胞的物理损伤而不是Cu2所致的毒性作用。总之,我们设计了Pickly@SpAcDX-PEG-VD 1142用于有效和有针对性的癌症治疗,这是一种非常有前途和新颖的纳米疗法,可以替代抗癌药物。总之,我们设想这种纳米复合材料的设计将为开发新型高效抗癌纳米材料开辟新的前景和见解。
祥鹄仪器在本论文中的使用过程
针状Zn-CuO纳米粒子的制备:采用国产高强度超声波装置(XH-300UL,北京祥鹄科技发展有限公司)制备了多刺纳米粒子。通常情况下,用搅拌将0.15g一水乙酸铜和0.055 g醋酸锌醛溶于10 mL双蒸馏水中,然后加入90 mL乙醇以维持体积比为9:1的乙醇/水溶液。超声作用5 min后,将0.8 mL氢氧化铵(28%~30%)注入细胞内,调节pH值至≈8,超声化学沉积过程继续1h(750 W,效率100%)。制备的氧化锌铜(Zn-CuO)NPs,用双蒸馏水离心洗涤两次,用乙醇洗涤一次,然后真空干燥。按上述工艺制备针状ZnCuO,用体积比为1:9的乙醇/水溶液制备针状ZnCuO。

